Naukowcy z Centrum Nowych Technologii UW wraz z badaczami z Uniwersytetu we Freiburgu odkryli nowy mechanizm regulacji syntezy białek, który wykorzystuje przełączniki redoks znajdujące się na rybosomach. Artykuł na temat odkrycia został opublikowany w czasopiśmie „Nature Communications”.
Mitochondria to organelle komórkowe. Często nazywane są „wewnątrzkomórkowymi elektrowniami”, ponieważ odpowiadają za wytwarzanie energii.
99% białek mitochondrialnych jest kodowanych przez geny znajdujące się w jądrze komórkowym i musi być syntetyzowana poza mitochondriami, a następnie importowana. Dr Ulrike Topf z grupy prof. Agnieszki Chacińskiej z CeNT UW próbowała dowiedzieć się, w jaki sposób mitochondria mogą sygnalizować swoje zapotrzebowanie na nowo syntetyzowane białka pochodzące spoza tych organelli.
Elektrownie wewnątrz komórek
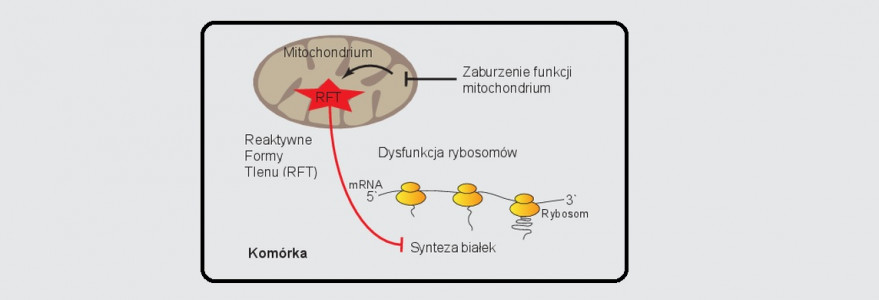
– We współpracy z grupą badaczy z Niemiec kierowaną przez prof. Bettinę Warscheid z Uniwersytetu we Freiburgu opisujemy nowy mechanizm, dzięki któremu dysfunkcyjne mitochondria regulują kluczowy proces komórkowy, którym jest synteza białek – mówi dr Ulrike Topf. – Co ciekawe, te komórkowe elektrownie robią to, informując maszynerię syntezy białek o swoich problemach i defektach, uwalniając reaktywne formy tlenu (RFT). Informacja ta prowadzi do spowolnienia syntezy białek komórkowych, co pozwala na szybszą regenerację i powrót do stanu homeostazy komórkowej – tłumaczy.
Dr Ulrike Topf, wykorzystując zaawansowane techniki biochemii białek i biologii komórki oraz drożdże Saccharomyces cerevisiae jako prosty organizm modelowy, zaobserwowała, że po zwiększeniu poziomu RFT globalna synteza białek ulegała hamowaniu. Odkryła molekularny przełącznik redoks, który służy do wyłączania syntezy białek w odpowiedzi na stres mitochondrialny. Następnie dr Łukasz Samluk wykazał, że regulacja syntezy białka przez wadliwe mitochondria istnieje również w komórkach ludzkich.
Patologie mitochondrialne
– Odkrycie, że mitochondria mogą sygnalizować swój stan za pośrednictwem RFT pochodzących z tych organelli i w ten sposób dostosować bezpośrednio globalną syntezę białek cytozolowych, pozwala na lepsze zrozumienie konsekwencji patologii mitochondrialnych i nieprawidłowego zwijania białek, charakterystycznego dla neurodegeneracji – mówi dr Topf.
Publikacja na stronie Nature Communications >>
Ulrike Topf#, Ida Suppanz#, Lukasz Samluk, Lidia Wrobel, Alexander Böser, Paulina Sakowska, Bettina Knapp, Martyna K. Pietrzyk, Agnieszka Chacinska* & Bettina Warscheid*. Quantitative proteomics identifies redox switches for global translation modulation by mitochondrially produced reactive oxygen species. (2018). Nature Communications. DOI: 10.1038/s41467-017-02694-8
# autorzy równorzędni, *autor korespondencyjny