Prof. Jacek Jemielity, dr hab. Joanna Kowalska oraz dr Anaïs Depaix z UW, we współpracy z naukowcami z University of California, wykazali, w jaki sposób aktywność enzymów w kondensatach wewnątrzkomórkowych przyczynia się do degradacji mRNA. Wyniki badań umożliwią dalszy rozwój terapii opartych na mRNA. Rezultaty prac naukowcy opisali na łamach czasopisma „Nature Chemical Biology”.
Cząsteczki mRNA posiadają na swoim końcu 5’ unikalną strukturę zwaną kapem lub czapeczką (z ang. cap), która pełni podstawową rolę w biosyntezie białka. Proces usuwania kapu jest etapem poprzedzającym degradację informacyjnego RNA. Zachodzi on w kondensatach białkowych (tzw. ciałkach P), które zawierają kwas nukleinowy oraz enzmy Dcp1/Dcp2, odpowiadające za degradację mRNA.
Naukowcy z Uniwersytetu Warszawskiego: prof. Jacek Jemielity z Centrum Nowych Technologii UW, dr hab. Joanna Kowalska oraz dr Anaïs Depaix z Wydziału Fizyki UW, we współpracy z badaczami z University of California w San Francisco, wykazali, w jaki sposób aktywność enzymu Dcp1/Dcp2 może ulegać „włączaniu” lub „wyłączaniu” w kondensatach. Wyniki prac zespołu zostały opublikowane w artykule „Biomolecular condensates amplify mRNA decapping by biasing enzyme conformation” na łamach czasopisma „Nature Chemical Biology”.
– W uproszczeniu kondensaty przypominają olej zawieszony w wodzie. Są one osobną ciekłą substancją, różnicą się od otaczającej je cytoplazmy. Odpowiadają one za rozdzielanie różnorodnych procesów biochemicznych zachodzących w komórkach – mówi prof. Jacek Jemielity z Centrum Nowych Technologii UW.
Aktywność enzymów
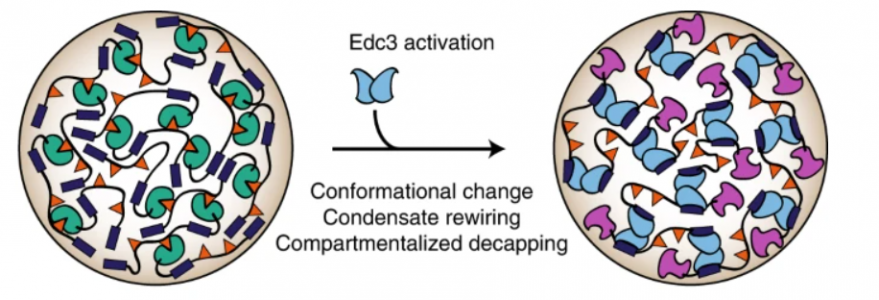
Badacze odkryli, że aktywność enzymu Dcp1/Dcp2 regulowana jest dzięki oddziaływaniom międzybiałkowym, które prowadzą do rozdziału faz ciecz-ciecz i tworzenia się kondensatów. Separacja enzymu Dcp1/Dcp2 utrwala go i hamuje proces usuwania kapu z mRNA. Dodanie kolejnego białka, Edc3, powoduje zmiany enzymu, które prowadzą do usuwania struktury kapu w mRNA przechowywanym w kondensatach i w konsekwencji umożliwiają degradację mRNA.
Wyniki badań wskazują, że struktury, w których zachodzi separacja faz, stanowią miejsca bardzo precyzyjnej aktywacji/dezaktywacji enzymów. Wnioski te przyczyniają się do zrozumienia, w jaki sposób w kondensatach białkowych mogą przebiegać czasem pozornie przeciwstawne procesy biochemiczne, które nie zostały dotychczas wyjaśnione.
Terapie mRNA
Uzyskanie rezultatów badań opisanych w artykule było możliwe dzięki opracowaniu przez zespół badaczy z UW metody oznaczania struktury mRNA znacznikami fluorescencyjnymi. Wyniki badań pomogą lepiej zrozumieć zmiany zachodzące w komórkach oraz umożliwią opracowanie kolejnych terapii mRNA.
– Procesy degradacji mRNA, w których uczestniczy enzym Dcp1/Dcp2, mają bezpośredni wpływ na wewnątrzkomórkową trwałość terapeutyków i szczepionek opartych o mRNA. Aby umożliwić obserwację tego procesu w kondensatach stworzyliśmy cząsteczki RNA specjalnie wyznakowane (świecące) innym kolorem na każdym z końców. Metoda ta może w przyszłości zostać również zastosowana do śledzenia degradacji terapeutyków na bazie mRNA, a w konsekwencji również do poszukiwania czynników spowalniających ten proces – mówi dr hab. Joanna Kowalska z Wydziału Fizyki UW.
Treść artykułu znajduje się na stronie czasopisma „Nature Chemical Biology”.
Spin-off UW ExploRNA Therapeutics
Prof. JacekJ emielity i dr hab. Joanna Kowalska od kilkunastu lat zajmują się modyfikacjami mRNA. W 2019 roku wraz z innymi naukowcami z Uniwersytetu Warszawskiego oraz Warszawskiego Uniwersytetu Medycznego założyli spółkę ExploRNA Therapeutics, spin-off Uniwersytetu Warszawskiego. Celem działalności spółki jest badanie skuteczności terapeutycznej nowych rozwiązań dotyczących modyfikowanego mRNA i wdrażanie ich w leczeniu.